2019年12月1日,新修订的《中华人民共和国药品管理法》以及我国首部疫苗法《中华人民共和国疫苗管理法》正式施行,两法对于我国医药产品从生产到使用整个流通与物流全过程做出了新的规定,为医药产品的质量安全、物流过程安全,以及流通过程中的数据安全等作出有效的保障。
同时,为了统一规范管理理念和部分落后用词、紧跟物流行业快速发展、匹配新法规的新规定,《药品冷链物流运作规范》国标开启了修订工作。在经历了标准启动会、调研等工作之后,该标准已经进入了征求意见阶段(征求意见材料请见附件)。标准修订任务重大,修改稿件更新较快,下面列出了标准新旧内容对比节选,先供大家查看:
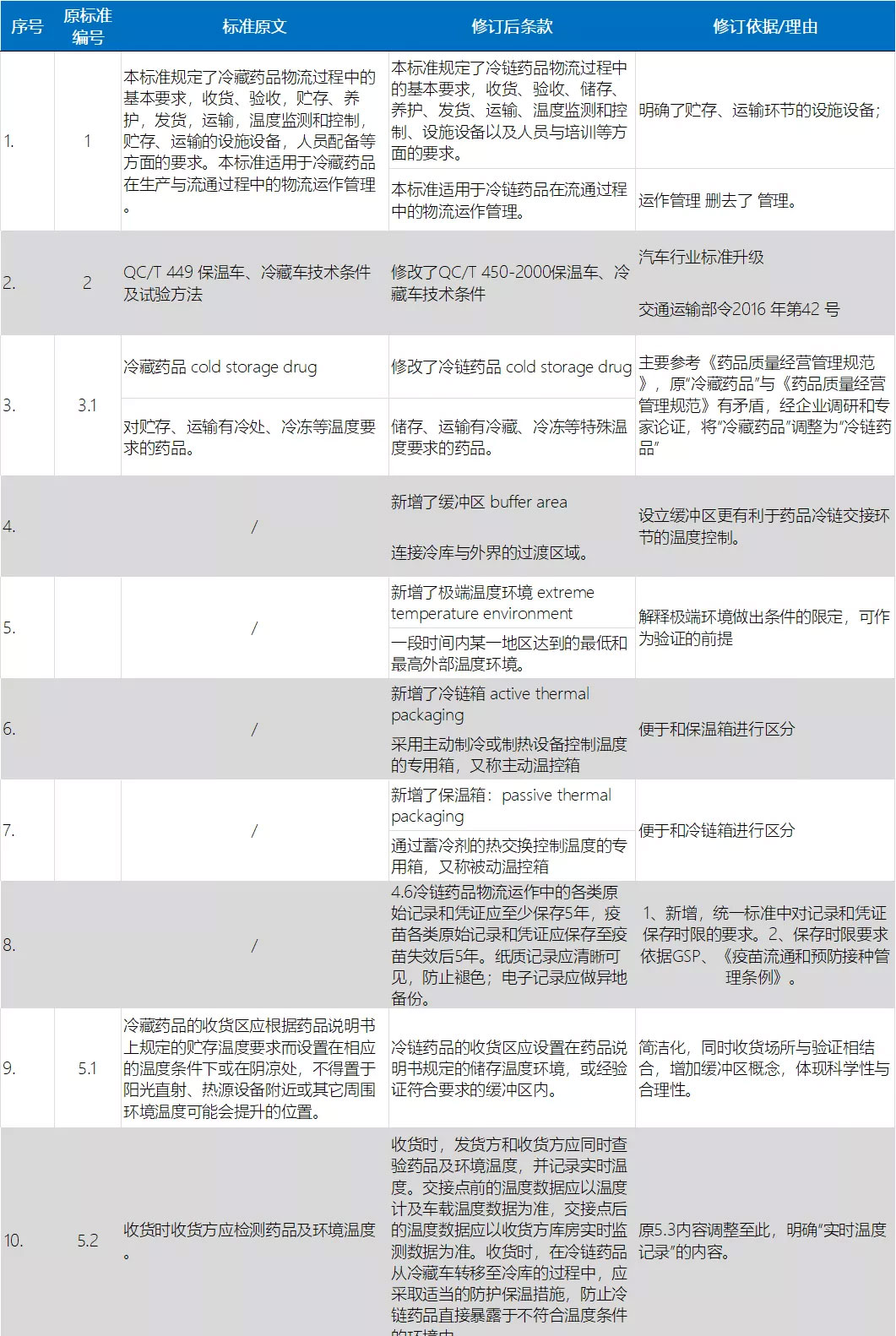
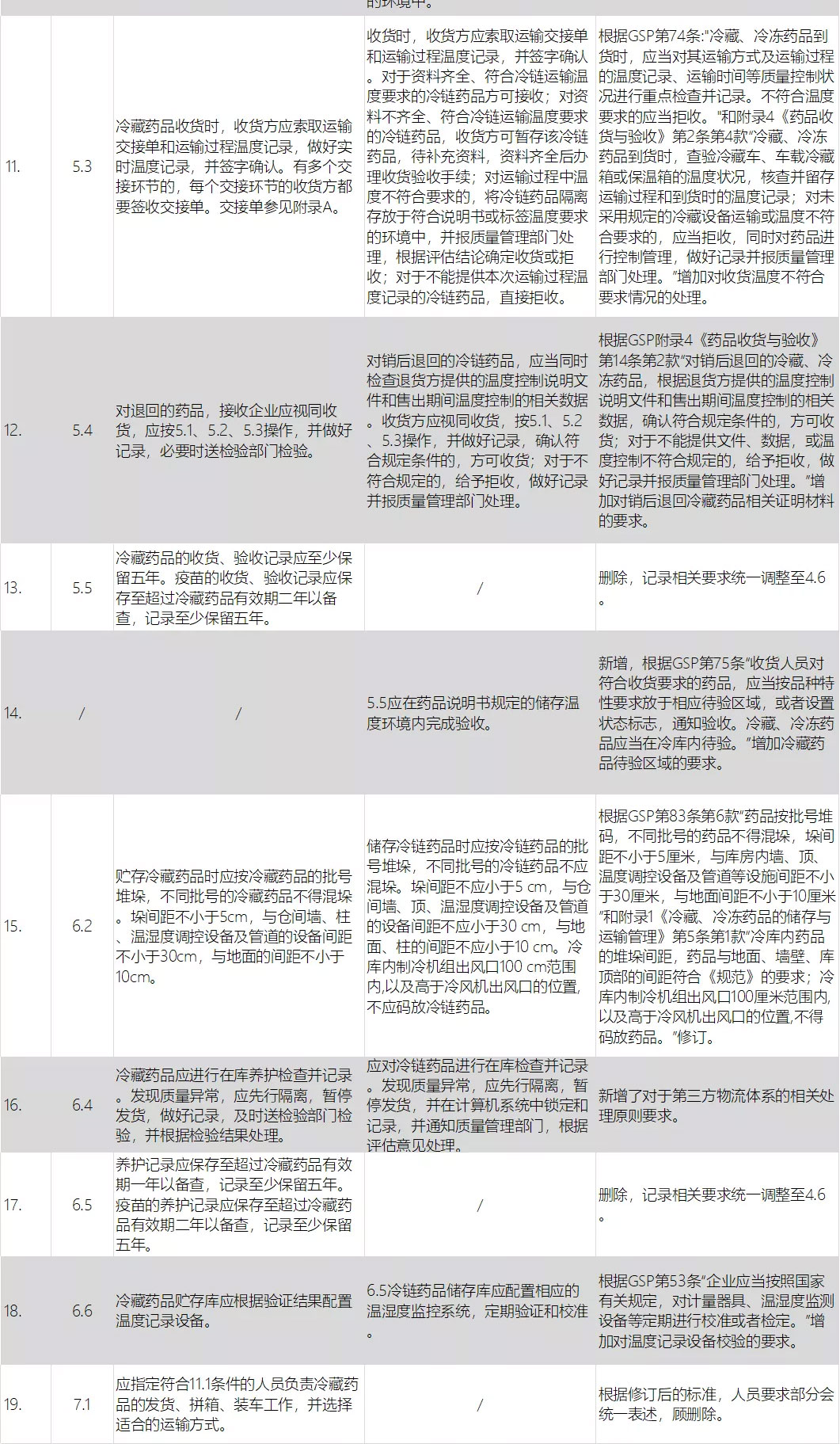
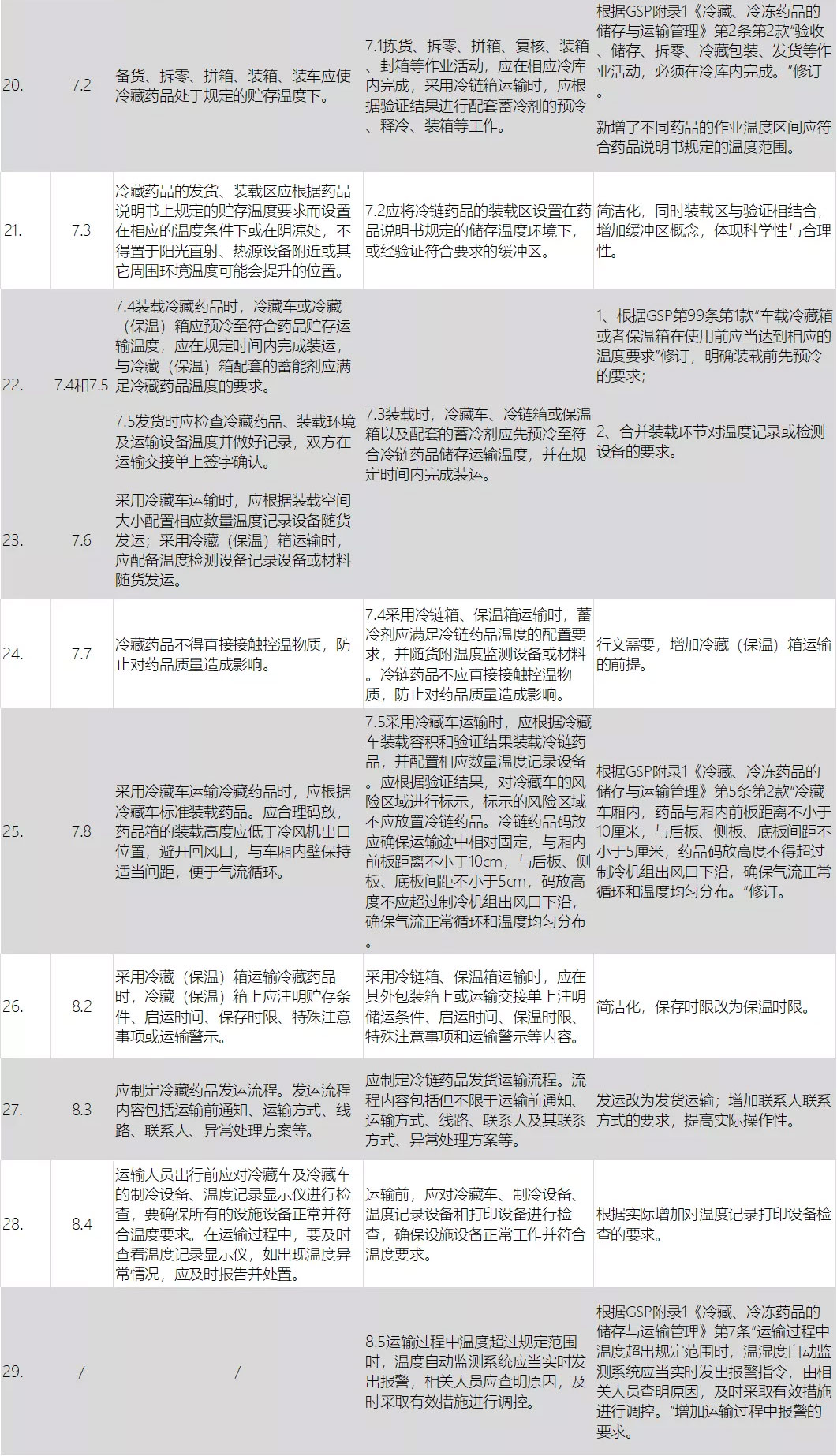
因此,为了更好的完成标准制定工作,加快标准修订速度,提高标准影响力,扩大标准参与范围,中物联医药物流分会定于8月14日13:30-17:30在江苏·徐州举办《药品冷链物流运作规范》国家标准研讨会,邀请各大企业、各位专家共同交流研讨,更好地完善标准内容。
一、时间、地点
2020年8月14日(周五)13:30-17:00
江苏·徐州
二、会议联系
联系人:刘洋、王晓晓
电 话:18401600052、15911188972
邮 箱:standard@cpl.org.cn
欢迎您的参会,参会回执表请于8月3日前反馈到秘书处。
附件下载:
1. 关于召开《药品冷链物流运作规范》国家标准研讨会的通知
2. 参会回执表
3.《药品冷链物流运作规范》国家标准(征求意见稿)
4.《药品冷链物流运作规范》国家标准(征求意见稿)编制说明
5.《药品冷链物流运作规范》国家标准(征求意见稿)意见反馈表